Questions / Réponses
par Tiphaine le Roy
La transplantation ou greffe fécale : où en est la recherche ?
Qu’est-ce que la transplantation fécale ?
Il est aujourd’hui largement reconnu que des anomalies de la composition du microbiote intestinal sont à l’origine de nombreuses maladies, aussi bien métaboliques, inflammatoires qu’infectieuses. Les chercheurs et médecins ont donc cherché à traiter ces maladies en rétablissant une composition normale du microbiote.
Plusieurs approches ont été explorées, dont la transplantation de microbiote fécal. Il s’agit d’ailleurs d’un très ancien traitement dont les origines remontent à la Chine du IVème siècle et dont le potentiel n’a été rigoureusement étudié en Occident qu’au début du 21ème siècle.
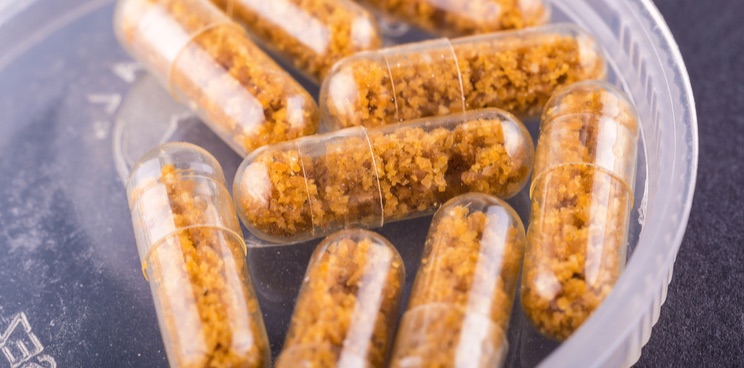
Ce traitement consiste à administrer au receveur malade les selles d’un donneur en bonne santé. Les selles du donneur sont diluées et filtrées avant d’être administrées au receveur. Plusieurs méthodes d’administration sont possibles : par coloscopie, par sonde nasogastrique ou encore sous forme de gélules.
Quelles maladies soigne-t-on aujourd’hui grâce à la transplantattion fécale ?
L’état d’avancement de la recherche n’est pas le même selon la pathologie concernée.
Dans le cas par exemple des colites récidivantes provoquées par la bactérie pathogène Clostridioides difficile (anciennement appelée Clostridium difficile), l’efficacité et la faible incidence des effets secondaires de la transplantation fécale sont totalement établis. Cette pathologie apparait suite à des perturbations majeures de la composition du microbiote intestinal, apparaissant le plus souvent suite à des traitements antibiotiques répétés visant à traiter une autre pathologie infectieuse (respiratoire, urinaire…). Entre 80 et 90% des patients infectés par cette bactérie pathogène sont guéris par la transplantation fécale, contre un taux de guérison de seulement 25 à 30 % avec les traitements antibiotiques dédiés1. A ce jour, l’infection à C. difficile est la seule maladie pour laquelle la transplantation fécale est un traitement standard2, approuvé par la Haute Autorité de Santé.
Pour quelles maladies est-ce que la transplantation est en cours d’étude dans le cadre d’essais cliniques ?
Dans le cas des autres pathologies, la transplantation fécale ne se fait que dans le cadre d’études cliniques.
Pour l’obésité et les maladies métaboliques telles que le diabète de type 2, seules quelques études portant sur moins de 20 à 30 patients ont été effectuées3,4. Elles révèlent la variabilité de l’implantation du microbiote des donneurs dans l’intestin des receveurs5. La moitié seulement des receveurs a eu une perte de poids et/ou une amélioration notable de son métabolisme du glucose. De plus, les effets positifs étaient de courte durée puisqu’ils avaient disparu 3 mois plus tard. Une des hypothèses pouvant expliquer ces résultats mitigés est qu’il est plus diffile de remplacer le microbiote du receveur par celui du donneur chez les receveurs souffrant d’obésité ou de maladies métaboliques que chez les receveurs souffrant de colites à C. difficile. En effet, le microbiote des patients atteints de colite est appauvri et affaibli, ce qui n’est pas le cas des patients souffrant d’obésité. Il semblerait également que tous les donneurs ne soient pas égaux en matière de transplantation fécale et que le microbiote de certains ait une meilleure capacité à coloniser le tube digestif des receveurs. Ce phénomène a aussi été constaté chez les patients souffrant de maladies chroniques inflammatoires de l’intestin comme la maladie de Crohn et la recto-colite hémoragiques : la transplantation fécale n’induit d’amélioration de la maladie que chez 25 à 30 % d’entre eux6.
Plusieurs phénomènes sont probablement à l’oeuvre, tels que l’action du système immunitaire intestinal sur le microbiote ou l’impact du régime alimentaire, mais il s’avère déjà que le microbiote des donneurs ayant permis une amélioration de la maladie chez les receveurs est plus riche, c’est-à-dire qu’il comporte plus d’espèces de bactéries différentes que celui des donneurs dont les selles n’ont pas permis d’améliorer l’état des receveurs.
Le potentiel thérapeutique de la transplantation de microbiote est également en cours d’étude pour le traitement de la réaction du greffon contre l’hôte lors de transplantations de cellules souches hématopoïétiques7. Cette complication grave, au pronostic sombre, a lieu lorsque les cellules immunitaires de la moelle osseuse du donneur attaquent les tissus du receveur. Le nombre de patients traités ne permet pas de tirer de conclusions définitives, mais les patients ayant un microbiote riche et diversifié après la transplantation sont entrés en rémission tandis que ceux qui avaient un microbiote appauvri en bactéries habituellement trouvées en grande quantité dans le microbiote (Bacteroides, Faecalibacterium et Bifidobacterium) mais riche en un groupe bactérien habituellement trouvé en petites quantités (Escherichia) a rechuté.
Les troubles neurologiques font aussi partie des pathologies pour lesquelles l’intérêt thérapeutique de la FMT est étudiée. Par exemple, dans le cas de l’autisme sévère, une étude portant sur 18 enfants a constaté une diminution significative des symptômes de l’autisme après avoir bénéficié d’une TMF8. Ces résultats sont d’autant plus prometteurs que l’amélioration des symptômes a perduré pendant au moins 2 ans9. Néanmoins, ces résultats doivent être confirmés par des études indépendantes incluant un plus grand nombre de patients et surtout comportant un groupe placebo.
Quels sont les effets indésirables ou complications de la transplantation ?
Quelle que soit la maladie initiale, deux types d’effets indésirables de la transplantation fécale sont possibles : ceux liés à la procédure en elle-même et ceux liés à la transmission d’une pathologie infectieuse du donneur au receveur.
Néanmoins, la plupart des études ont constaté une très bonne tolérance de la transplantation fécale à court et long terme ainsi que la rareté des effets secondaires indésirables. Une étude de plus de 1000 patients ayant reçu une transplantation fécale par colonoscopie ou par tube nasoduodénal montre que seulement 0.97 % des patients ont été victimes d’une complication menant à une hospitalisation, par exemple un accident d’anesthésie lors de l’administration par coloscopie10. Les autres effets indésirables liés à la transplantation de microbiote fécal sont bénins et transitoires, tels que des ballonnements, des diarrhées, des flatulences et des douleurs abdominales voire des vomissements.
Le second type de complication de la transplantation fécale est à rattacher aux selles des donneurs qui peuvent véhiculer des agents infectieux, un dépistage minutieux de la présence de pathogènes dans le microbiote du donneur est donc indispensable. C’est un point crucial dramatiquement illustré par deux cas de septicémie, dont un fatal, rapportés récemment chez des patients immunodéprimés ayant reçu une transplantation fécale aux États-Unis11. Ces deux patients ont développé une infection à Escherichia coli ST-131 O25B, une souche connue pour sa résistance à de multiples antibiotiques. Le donneur s’est par la suite révélé être porteur sain de la souche isolée chez les deux patients. Il faut souligner que la recherche de bactéries antibio-résistantes dans les selles du donneur n’avait pas été effectuée préalablement au don de selles, comme cela se fait systématiquement en Europe et plus particulièrement en France.
L’importance du dépistage de pathogènes afin de préserver le receveurs d’infections graves est également illustré par le fait que jusqu’à 50 % des malades du COVID-19, y compris asymptomatiques, ont des taux détectables d’ARN viral dans leurs selles12. En Europe la sélection des donneurs est particulièrement stringente et de nombreux dépistages sont effectués, ainsi seulement 3 % des donneurs potentiels sont retenus. Ceci garantit la sécurité du receveur mais augmente considérablement la difficulté de mise en oeuvre et les coût de la transplantation de microbiote fécale et contribue à limiter son utilisation13.
En l’état actuel des connaissances, il apparait donc que la transplantation fécale est très efficace dans le traitement des colites à C. difficile mais nettement moins dans d’autres maladies telles que l’obésité et les maladies chroniques inflammatoires de l’intestin. Cette variabilité de l’efficacité selon les patients est très probablement à mettre en lien avec la composition du microbiote du donneur et du receveur. Il semble en effet que la capacité de colonisation du microbiote du donneur dépasse la résistance à l’implantation d’un nouveau microbiote chez le receveur lorsque le donneur a un microbiote plus riche que le receveur. Il reste encore de nombreuses zones d’ombre à explorer afin d’améliorer l’efficacité de la transplantation fécale. A ce jour, les impacts respectifs de la méthode de préparation et de conservation du microbiote du donneur, du nombre d’administrations de selles, de l’appariement donneur-receveur et d’une intervention nutritionnelle ou médicamenteuse simultanément la transplantation fécale sont encore inconnus mais ouvrent des perspectives de recherche prometeuses.
Bibliographie
- van Nood, E. et al. Duodenal Infusion of Donor Feces for Recurrent Clostridium difficile. Engl. J. Med. 368, 407–415 (2013).
- Sokol, H. et al. Transplantation de microbiote fécal dans le cadre des infections à Clostridium difficile récidivantes : recommandations pour la pratique clinique courante. Hépato Gastro 287–290 (2015).
- Vrieze, A. et al. Transfer of Intestinal Microbiota From Lean Donors Increases Insulin Sensitivity in Individuals With Metabolic Syndrome. Gastroenterology 143, 913-916.e7 (2012).
- Kootte, R. S. et al. Improvement of Insulin Sensitivity after Lean Donor Feces in Metabolic Syndrome Is Driven by Baseline Intestinal Microbiota Composition. Cell Metab. 26, 611-619.e6 (2017).
- Li, S. S. et al. Durable coexistence of donor and recipient strains after fecal microbiota transplantation. Science 352, 586 (2016).
- Kump, P. et al. The taxonomic composition of the donor intestinal microbiota is a major factor influencing the efficacy of faecal microbiota transplantation in therapy refractory ulcerative colitis. Pharmacol. Ther. 47, 67–77 (2018).
- DeFilipp, Z., Hohmann, E., Jenq, R. R. & Chen, Y.-B. Fecal Microbiota Transplantation: Restoring the Injured Microbiome after Allogeneic Hematopoietic Cell Transplantation. Blood Marrow Transplant. 25, e17–e22 (2019).
- Kang, D.-W. et al. Microbiota Transfer Therapy alters gut ecosystem and improves gastrointestinal and autism symptoms: an open-label study. Microbiome 5, 10 (2017).
- Kang, D.-W. et al. Long-term benefit of Microbiota Transfer Therapy on autism symptoms and gut microbiota. Rep. 9, 5821 (2019).
- Rossen, N. G. Fecal microbiota transplantation as novel therapy in gastroenterology: A systematic review. World J. Gastroenterol. 21, 5359 (2015).
- DeFilipp, Z. et al. Drug-Resistant E. coli Bacteremia Transmitted by Fecal Microbiota Transplant. N. Engl. J. Med. (2019) doi:10.1056/NEJMoa1910437.
- Ianiro, G. et al. Screening of faecal microbiota transplant donors during the COVID-19 outbreak: suggestions for urgent updates from an international expert panel. Lancet Gastroenterol. Hepatol. 5, 430–432 (2020).
- Kassam, Z. et al. Donor Screening for Fecal Microbiota Transplantation. N. Engl. J. Med. 381, 2070–2072 (2019).